viernes, 6 de noviembre de 2009
La interferencia por los implantes mamarios en la mamografía
Según un artículo de la Revista de la Asociación Médica Americana (JAMA) de enero de 2004, se ha demostrado que los implantes mamarios han impedido la detección del cáncer. El estudio demostró que:
La mamografía no logró detectar un 55% de casos de cáncer de mama en mujeres con implantes, comparado con sólo un 33% en mujeres sin implantes;
Los implantes mamarios dificultan la interpretación de las mamografías debido a que los implantes aparecen como una “masa blanca sólida” que bloquea la visualización del tejido mamario.5
Según la Food and Drug Administration (FDA) de EE.UU.:
Los implantes mamarios presentan una complicación frecuente llamada contractura capsular en la cual se desarrolla un tejido cicatrizante doloroso alrededor del implante, lo que hace que la mama se endurezca y se sensibilice (hasta terriblemente dolorosa) al tacto. Cuando esto sucede, la mamografía puede ser extremadamente dolorosa o imposible debido a la compresión que implica el procedimiento.6
El 62.1% de las complicaciones asociadas con los implantes mamarios y las mamografías se debe a la ruptura del implante mamario durante el procedimiento. Durante la mamografía, se informó sobre la ruptura tanto de implantes mamarios salinos e implantes con gel de silicona, como de implantes mamarios salinos.7
¿Qué debe hacer si los implantes mamarios son un problema?Recuerde, la mamografía salva vidas. Aún si tiene implantes mamarios, siga haciéndose las mamografías de rutina para la detección del cáncer de mama tal como se lo recomendó su médico y realícese autoexámenes mamarios mensuales. Sin embargo, debe considerar lo siguiente:
Al programar una mamografía, asegúrese de comunicarle al centro de mamografías que tiene implantes mamarios. Es importante que lo haga ya que el radiólogo o el técnico que realice la mamografía deberá tomar planos extra de la mama.
Es importante comprender que cuando se utilizan técnicas de mamografía específicas de implantes (conocidas como "planos del desplazamiento del implante”), una porción del tejido mamario permanece oculta por los implantes.8
Los procedimientos especiales de la mamografía o las imágenes adicionales necesarias durante la mamografía someterán a las mujeres con implantes mamarios a una dosis doble de radiación como mínimo por mamografía en comparación con el procedimiento normal.9
La Sociedad Americana de Cirugía Plástica y Reconstructiva junto con la Food and Drug Administration (FDA) de los EE.UU. recomiendan que las mujeres con implantes mamarios sean derivadas a prestadores de asistencia médica especialistas en realizar mamografías en pacientes con implantes.10
Mamografía Digital
Sharp Memorial Outpatient Pavilion ahora ofrece a las mujeres que están acudiendo para sus mamogramas de rutina lo último disponible en tecnología de diagnóstico, la mamografía digital. El nuevo sistema de mamografía digital Selenia™ incorpora una revolucionaria tecnología de imágenes que proporciona a las pacientes la más alta calidad de cuidado en la prevención y detección temprana del cáncer de seno.
La mamografía digital utiliza computadoras y detectores digitales especialmente diseñados para producir una imagen que puede ser proyectada en un monitor de computadora de alta resolución, y trasmitido y archivado igual que los expedientes de computadora. Esta tecnología permite a los radiólogos ver las imágenes de rayos X en cuestión de segundos. Pueden ajustar la brillantez, cambiar el contraste, y magnificar áreas específicas para detectar pequeñas calcificaciones, o masas, y otros cambios que pudieran ser señales de cáncer en etapa temprana. La capacidad de manipular imágenes es uno de los principales beneficios de la tecnología digital.
Para suplementar esta tecnología, el Outpatient Pavilion de Sharp Memorial también ofrece Detección Asistida por Computadora (CAD por sus siglas en inglés) como parte de sus servicios completos de diagnóstico. CAD proporciona una “segunda lectura” del mamograma digital por computadora y hace destacar las características comúnmente asociadas con cáncer de seno. Al activarse, indica anomalías para ayudar al radiólogo a detectar el cáncer de seno en etapa temprana. CAD es, en esencia, un segundo par de ojos para apoyar y reforzar el criterio del radiólogo.
Para hacer más agradable la experiencia del mamograma, el Outpatient Pavilion ha empezado a usar el singular MammoPad. Se trata de un cojín con adhesivo atrás, de un solo uso, el cual proporciona calidez, confort y limpieza.
Ventajas
Menos necesidad de repetir las pruebas debido a que faltó o sobró exposición
Mayor precisión de diagnóstico que las técnicas tradicionales, en particular para mujeres menores de 50 años y en mujeres con tejido denso
Menos radioactividad para las pacientes
Menos tiempo en espera para el procedimiento
Mamografías selectivas de detección: preguntas y respuestas
Una mamografía selectiva de detección es una radiografía del seno que se usa para detectar cambios en el seno en mujeres que no presentan signos o síntomas de cáncer de mama. Se dice selectiva porque ordinariamente se elige tener esta prueba de detección por razones de prevención y no porque haya algún síntoma. Generalmente se requieren dos radiografías de cada seno. Con una mamografía, es posible detectar un tumor que no se puede palpar o encontrar microcalcificaciones (pequeños depósitos de calcio en el seno), los cuales a veces son una indicación de la presencia de cáncer de mama.
¿Cuál es la diferencia entre una mamografía selectiva de detección y una mamografía de diagnóstico?
Una mamografía de diagnóstico es una radiografía del seno que se usa para ver si la paciente tiene cáncer de mama después de haberse encontrado un bulto u otro signo o síntoma de cáncer de seno. Los signos de cáncer de mama pueden ser el dolor, engrosamiento de la piel, secreción del pezón, o un cambio en el tamaño o forma del seno. La mamografía de diagnóstico puede usarse también para evaluar los cambios que se hayan encontrado en una mamografía selectiva de detección o para ver el tejido de seno cuando es difícil obtener una mamografía selectiva de detección debido a circunstancias especiales, como la presencia de implantes en el seno (vea la pregunta 13 ). Una mamografía de diagnóstico se lleva más tiempo que una mamografía selectiva de detección porque requiere más radiografías para obtener vistas del seno desde varios ángulos. El técnico puede amplificar un área sospechosa para producir una imagen detallada que ayude al médico a hacer un diagnóstico preciso.
¿Cuándo recomienda el Instituto Nacional del Cáncer (NCI) que las mujeres se hagan mamografías selectivas de detección?
• Las mujeres de 40 años o más se deberán hacer mamografías cada 1 ó 2 años.
• Las mujeres que tienen un riesgo mayor que el promedio de cáncer de mama deberán hablar con un profesional médico acerca de la necesidad de hacerse mamografías antes de los 40 años y de la frecuencia.
¿Cuáles son los factores que ponen a la mujer en un riesgo mayor de padecer cáncer de mama?
El riesgo de cáncer de mama aumenta gradualmente conforme la mujer envejece. Sin embargo, el riesgo no es el mismo para todas las mujeres. La investigación ha demostrado que los siguientes factores aumentan las probabilidades de una mujer de padecer esta enfermedad:
• Antecedentes personales de cáncer de mama: Las mujeres que han tenido cáncer de mama tienen más probabilidad de padecer un segundo cáncer de mama.
• Antecedentes familiares: Las probabilidades de una mujer de padecer cáncer de mama aumentan si su madre, hermana o hija tiene antecedentes de cáncer de mama (especialmente si el diagnóstico se hizo antes de los 50 años de edad).
• Algunos cambios del seno en la biopsia: Un diagnóstico de hiperplasia atípica (una afección que no es cancerosa, en la cual las células tienen características anormales y son numerosas) o de carcinoma lobulillar in situ (CLIS) (células anormales que se encuentran en los lobulillos del seno) aumenta el riesgo de cáncer de mama de una mujer. Las mujeres que han tenido dos o más biopsias del seno a causa de otros estados benignos tienen también una mayor probabilidad de padecer cáncer de mama. Este aumento es debido a la situación que condujo a hacerse la biopsia y no a la biopsia misma.
• Alteraciones genéticas (mutaciones): Alteraciones específicas en ciertos genes (BRCA1, BRCA2 y otros) aumentan el riesgo de cáncer de mama. Estas alteraciones son raras; se estima que no llegan a un 10 por ciento de todos los cánceres de seno.
• Antecedentes de reproducción y menstruación: Las mujeres que empezaron a menstruar a una edad temprana (antes de los 12 años) o pasaron por la menopausia después de los 55 años de edad, o que nunca tuvieron hijos o los tuvieron después de los 30 años de edad tienen un riesgo mayor de padecer cáncer de mama.
• Uso de terapia hormonal por un largo plazo para la menopausia: Las mujeres que usan la terapia hormonal de combinación de estrógeno y progestina para la menopausia durante más de 5 años tienen una mayor probabilidad de presentar cáncer de mama.
• Densidad del seno: Los senos parecen densos en una mamografía si contienen muchas glándulas y ligamentos (lo que se llama tejido denso) y no tienen mucho tejido graso. Ya que los cánceres de seno tienden a presentarse en el tejido denso del seno (no en el tejido graso), las mujeres de más edad cuyas mamografías muestran tejido más denso tienen un riesgo mayor de cáncer de mama. Las anormalidades en los senos densos pueden detectarse con más dificultad en una mamografía.
• Radioterapia (“terapia con rayos X”): Las mujeres que tuvieron radioterapia al pecho (incluyendo los senos) antes de los 30 años de edad tienen un riesgo mayor de padecer cáncer de mama. Esto incluye a mujeres que fueron tratadas a causa de linfoma de Hodgkin. Los estudios indican que en cuanto más joven era la mujer cuando recibió su tratamiento, mayor es su riesgo de presentar cáncer de mama más tarde en su vida.
• Dietilestilbestrol, DES: Algunas mujeres embarazadas en los Estados Unidos recibieron dietilestilbestrol entre 1940 y 1971. (Ya no se administra este fármaco a las mujeres embarazadas). Las mujeres que tomaron DES durante el embarazo pueden tener un riesgo ligeramente mayor de padecer cáncer de mama. Están en estudio los posibles efectos en sus hijas.
• Peso corporal: Según los estudios, la probabilidad de presentar cáncer de mama después de la menopausia es mayor entre las mujeres que tienen sobrepeso o que son obesas.
• Nivel de actividad física: Las mujeres que son inactivas físicamente a lo largo de su vida pueden tener un mayor riesgo de cáncer de mama. Ser activa puede reducir el riesgo al prevenir el aumento de peso y la obesidad.
• Alcohol: Los estudios sugieren que cuanto más alcohol toma una mujer, mayor es su riesgo de padecer cáncer de mama.
¿Cuáles son las probabilidades de que una mujer en Estados Unidos padezca cáncer de mama?
La edad es el factor más importante de riesgo para el cáncer de mama. En cuanto más edad tiene la mujer, mayor es su probabilidad de padecer cáncer de mama. Las tasas actuales sugieren que el 13,2 por ciento de las mujeres (una de cada ocho) nacidas hoy serán diagnosticadas con cáncer de mama en algún momento de su vida. Esta estadística se basa en los promedios de la población. Sin embargo, la probabilidad estimada de ser diagnosticada con cáncer de mama en grupos específicos de edad y durante periodos específicos de tiempo puede ser una manera más informativa para considerar el riesgo de cáncer de mama. Las estimaciones de padecer cáncer de mama en intervalos de diez años —vea más abajo—toman en cuenta que no todas las mujeres alcanzan la tercera edad, cuando el riesgo de cáncer de mama es mayor.
La probabilidad de que una mujer sea diagnosticada con cáncer de mama es:
de 30 a 39 años. . .0,44 por ciento (1 de cada 229)de 40 a 49 años. . .1,46 por ciento (1 de cada 68)de 50 a 59 años. . .2,73 por ciento (1 de cada 37)de 60 a 69 años. . .3,82 por ciento (1 de cada 26)
La mayoría de los casos de cáncer de mama ocurren en mujeres mayores de 50 años de edad; el número de casos es especialmente alto en mujeres mayores de 60 años. El cáncer de mama es relativamente raro en mujeres menores de 40 años de edad. La hoja informativa del NCI Probability of Breast Cancer in American Women tiene más información acerca del riesgo de padecer cáncer de mama en el transcurso de la vida. Esta hoja informativa se encuentra en http://www.cancer.gov/cancertopics/factsheet/Detection/probability-breast-cancer en Internet.
¿Cuál es el mejor método para detectar el cáncer de mama lo antes posible?
El hacerse regularmente una mamografía de buena calidad y un examen clínico de los senos (un examen realizado por un profesional médico) es el método más efectivo para detectar cáncer de mama temprano. Como cualquier examen, las mamografías tienen tanto beneficios como limitaciones. Por ejemplo, algunos cánceres no pueden ser detectados por una mamografía pero pueden encontrarse por el examen de los senos.
El examen de los senos que se hace una mujer a sí misma buscando bultos o cambios no acostumbrados se llama autoexamen del seno (breast self-exam, BSE). Hasta ahora, los estudios no han demostrado que el autoexamen del seno por sí mismo reduce el número de muertes por cáncer de mama. El autoexamen del seno no debe reemplazar los exámenes clínicos de los senos ni las mamografías de rutina.
¿Cuáles son los beneficios de las mamografías selectivas de detección?
Varios estudios grandes que se han llevado a cabo en el mundo han demostrado que los exámenes de detección del cáncer de mama usando mamografías reducen el número de muertes por cáncer de mama en mujeres que tienen de 40 a 69 años de edad; en especial, las que tienen más de 50 años. Los estudios que se han realizado hasta ahora no han demostrado un beneficio de las mamografías selectivas de detección regulares o de las mamografías selectivas de detección de base (una mamografía que se usa como comparación) en mujeres menores de 40 años.
¿Cuáles son algunas de las limitaciones de las mamografías selectivas de detección?
• Detectar el cáncer no siempre significa salvar vidas: Aun cuando la mamografía puede detectar tumores que no se pueden palpar, el detectar un tumor pequeño no siempre significa que se salvará la vida de una mujer. Puede ser que la mamografía no ayude a una mujer con un cáncer de crecimiento rápido o agresivo que ya se haya diseminado a otras partes del cuerpo antes de ser detectado.
• Resultados negativos falsos: Éstos ocurren cuando las mamografías parecen normales aun cuando hay realmente presente cáncer de mama. En general, las mamografías dejan de detectar hasta un 20 por ciento de los cánceres de seno que están presentes al momento de hacerse esta prueba de detección. Los resultados negativos falsos son más comunes en las mujeres jóvenes que en las mujeres mayores ya que los senos densos de las mujeres jóvenes dificultan más la detección del cáncer de mama en las mamografías. Conforme envejecen las mujeres, sus senos se hacen más grasos (por lo tanto, menos densos) y los cánceres de seno se pueden detectar con más facilidad en las mamografías selectivas de detección.
• Resultados positivos falsos: Éstos ocurren cuando el radiólogo lee las mamografías como anormales, pero en realidad no hay cáncer presente. Aunque todas las mamografías anormales se deberían seguir con pruebas adicionales (con mamografía de diagnóstico, ecografía o con una biopsia) para determinar si hay cáncer presente. Los resultados positivos falsos son más comunes en las mujeres jóvenes, en mujeres que han tenido antes biopsias del seno, en mujeres con antecedentes familiares de cáncer de mama y en mujeres que están tomando estrógeno (por ejemplo, como terapia de reemplazo hormonal).
¿Qué es el Sistema de Reporte y Base de Datos de Estudios de Imágenes de la Mama (BI-RADS®)?
El Colegio Estadounidense de Radiología (American College of Radiology, ACR) ha establecido un método uniforme para que los radiólogos reporten los resultados de las mamografías. El sistema, llamado BI-RADS, incluye siete categorías o niveles generalizados. Cada categoría del BI-RADS tiene un plan de seguimiento para ayudar a los radiólogos y a otros médicos a que manejen adecuadamente el cuidado de las pacientes.
Sistema de Reporte y Base de Datos de Estudios de Imágenes de la Mama(BI-RADS)
Categoría
Evaluación
Seguimiento
0
Requiere una evaluación adicional con imágenes
Requiere más estudios de imágenespara poder asignar una categoría
1
Negativo
Continuar las mamografías anualesde detección (para mujeres mayoresde 40 años)
2
Resultado benigno (no canceroso)
Continuar las mamografías anualesde detección (para mujeres mayoresde 40 años)
3
Probablemente benigno
Hacerse mamografía deseguimiento a los seis meses
4
Anormalidad sospechosa
Puede requerir una biopsia
5
Muy probable que sea maligno (cáncer)
Requiere una biopsia
6
Resultados de biopsiaobtenidos—condición maligna comprobada (cáncer)
Biopsia confirma presencia decáncer antes de iniciar tratamiento
Hay más información disponible sobre el BI-RADS en el sitio web del ACR en http://www.acr.org/ en Internet o al llamar al teléfono 1–800–227–5463 (1–800–ACR–LINE) del Colegio Estadounidense de Radiología.
¿Qué sucede si la mamografía da como resultado la detección de carcinoma ductal in situ (CDIS)?
En los últimos 30 años, el progreso en las mamografías ha hecho posible que se detecte un número mayor de anormalidades en el tejido que se llaman carcinomas ductales in situ (CDIS), los cuales son células anormales confinadas a los conductos de leche del seno. Las células no han invadido el tejido de seno del derredor. El CDIS no forma por lo general un bulto, por lo que no puede detectarse durante un examen clínico del seno. Sin embargo, la mamografía puede detectar ochenta por ciento de los casos de CDIS. Algunos de estos casos se convierten más tarde en cánceres invasores.
No es posible predecir cuáles casos de carcinomas ductales in situ se convertirán en cáncer invasor. Por lo cual, los CDIS se extirpan quirúrgicamente. Hasta hace poco, los CDIS se trataban a menudo con mastectomía, pero la cirugía conservadora de seno (cirugía de preservación del seno más radioterapia) es ahora la práctica normal para muchas mujeres con CDIS. El tamoxifeno puede también usarse. Las mujeres que han sido diagnosticadas con carcinoma ductal in situ deberán hablar con su médico para tomar una decisión informada acerca del tratamiento.
¿Cuánto cuesta una mamografía?
Las mamografías selectivas de detección cuestan generalmente entre $50 y $150. La mayoría de los estados ahora tienen leyes que requieren que las compañías de seguros médicos reembolsen todo o una parte del costo de estas mamografías. Las compañías de seguros o los proveedores de servicios médicos pueden proveer los detalles.
Todas las mujeres de 40 años y más que tienen Medicare pueden hacerse una mamografía de detección cada año. Medicare pagará también por una mamografía de base para mujeres de 35 a 39 años de edad. No se requiere un deducible para este beneficio, pero las beneficiarias de Medicare son responsables del pago del 20 por ciento de la cantidad aprobada por Medicare. La información acerca de lo que cubre Medicare se puede obtener en Internet en http://www.medicare.gov o llamando a la línea directa de Medicare: 1–800–633–4227 (1–800–MEDICARE). Para personas sordas o con problemas de audición, el número es 1–877–486–2048.
Algunos programas locales y estatales de salud así como algunas empresas proveen mamografías gratis o a bajo costo. Por ejemplo, los Centros de Control y Prevención de Enfermedades (CDC) coordinan el Programa Nacional de Detección Temprana del Cáncer de Mama y de Cérvix (National Breast and Cervical Cancer Early Detection Program, NBCCEDP). Este programa proporciona servicios de exámenes selectivos de detección, incluso exámenes clínicos de senos y mamografías, a mujeres de bajos ingresos en todos los Estados Unidos y varios de sus territorios. La información para llamar a los programas locales está disponible en el sitio web de los CDC en http://apps.nccd.cdc.gov/cancercontacts/nbccedp/contacts.asp, o en el teléfono de los CDC 1–888–232–4636 (1–888–CDC–INFO). Información sobre programas de mamografías selectivas de detección a precio reducido o gratis está disponible también por medio del Servicio de Información sobre el Cáncer (CIS) del Instituto Nacional del Cáncer (NCI) en el teléfono 1–800–422–6237 (1–800–4–CANCER).
¿En dónde puede una mujer hacerse una mamografía de buena calidad?
Las mujeres pueden hacerse una mamografía de buena calidad en las clínicas de seno, en el departamento de radiología de los hospitales, en unidades móviles, en empresas privadas de radiología y en los consultorios de los médicos.
La Ley de Normas de Calidad de la Mamografía (MQSA) es una ley federal designada para asegurar que las mamografías son seguras y confiables. Por medio de esta ley, todos los establecimientos en donde se realizan mamografías en Estados Unidos deben cumplir con estrictas normas de calidad, deben estar acreditados por la Food and Drug Administration (FDA) y deben ser inspeccionados cada año. La FDA asegura que los establecimientos de mamografías de todo el país satisfacen las normas de la Ley de Normas de Calidad de la Mamografía. Estas normas se aplican al siguiente personal en un establecimiento de mamografías:
• el técnico que toma la mamografía• el radiólogo que interpreta la mamografía• el físico médico que prueba el equipo de mamografía
Las mujeres pueden preguntar a sus doctores o al personal del establecimiento de mamografías sobre el certificado de la FDA antes de hacer su cita. Se requiere que todos los establecimientos de mamografías exhiban su certificado de la FDA. Las mujeres deberán buscar el certificado de la MQSA en el establecimiento de mamografías y verificar la fecha de vencimiento. Las regulaciones de la MQSA requieren también que los establecimientos de mamografías den a las pacientes un informe que sea fácil de leer sobre los resultados de su mamografía.
La información sobre los establecimientos certificados por la Food and Drug Administration en su localidad está disponible por medio del Servicio de Información sobre el Cáncer del Instituto Nacional del Cáncer: 1–800–422–6237 (1–800–4–CANCER).
También, en el sitio web de la FDA hay una lista de estos establecimientos en http://www.fda.gov/cdrh/mammography/certified.html en Internet.
¿Qué deberán hacer las mujeres que tienen implantes en los senos con respecto a las mamografías selectivas de detección?
Las mujeres con implantes en los senos deberán continuar teniendo mamografías. (Las mujeres a las que se puso un implante a consecuencia de cirugía por cáncer de mama deberán preguntar al médico si es necesaria una mamografía del seno reconstruido.) Es importante hacer saber al establecimiento que una mujer tiene implantes en los senos cuando se hace la cita para la mamografía. El técnico y el radiólogo deben tener experiencia en tomar radiografías de pacientes con implantes en los senos. Es posible que los implantes oculten algo de tejido del seno, lo cual dificulta más para el radiólogo el detectar alguna anormalidad en la mamografía. Si el técnico que realiza el procedimiento sabe que la mujer tiene un implante en el seno, se pueden tomar algunas medidas para asegurar que se vea la mayor cantidad posible de tejido de seno en la mamografía.
¿Qué es la mamografía digital? ¿En qué se diferencia de la mamografía convencional (película de radiografía)?
Tanto la mamografía digital como la convencional utilizan la radiación de rayos X para producir una imagen del seno; sin embargo, la mamografía convencional registra la imagen directamente en película, mientras que la mamografía digital toma una imagen electrónica del seno y la almacena directamente en una computadora. Esto permite que se mejoren, amplíen o manipulen los datos capturados para una evaluación posterior. La diferencia entre la mamografía convencional y la digital es semejante a la diferencia entre una cámara fotográfica de rollo y una cámara digital. Aparte de la diferencia en la forma de grabar y almacenar la imagen, no hay ningún otra diferencia entre las dos.
En enero de 2000, la FDA aprobó el primer sistema de mamografía digital. En septiembre de 2005, se publicaron los resultados preliminares de un estudio clínico grande (estudio de investigación) de comparación de la mamografía digital con la convencional. Los resultados no muestran que haya una diferencia entre las mamografías digitales y las convencionales para detectar cáncer de seno en la población general de mujeres del estudio. Sin embargo, las mujeres con senos densos que son pre o perimenopáusicas (mujeres que tuvieron su última menstruación dentro de los doce meses de sus mamografías) o que son menores de 50 años pueden beneficiarse de la mamografía digital en comparación con la convencional.
La mamografía digital permite que el radiólogo ajuste, guarde y recupere electrónicamente las imágenes digitales. Esto puede ofrecer las siguientes ventajas sobre la mamografía convencional:
• Se pueden tener consultas a larga distancia con más facilidad con otros especialistas en mamografía;
• Es posible notar diferencias sutiles entre los tejidos normales y anormales;
• La mamografía digital puede reducir el número de procedimientos necesarios de seguimiento; y
• La necesidad de menos exposiciones con la mamografía digital puede reducir aún más los niveles ya bajos de radiación.
Actualmente, la mamografía digital puede hacerse sólo en establecimientos certificados para practicar la mamografía convencional y que han recibido aprobación de la FDA para ofrecer mamografías digitales. El procedimiento para hacerse una mamografía con un sistema digital es el mismo que con mamografía convencional.
¿Qué otros tipos de tecnología están siendo desarrollados para exámenes selectivos de cáncer de mama?
El Instituto Nacional del Cáncer está apoyando el desarrollo de varias tecnologías nuevas para detectar tumores de seno. Esta investigación abarca desde métodos que se están desarrollando en laboratorios de investigación hasta los que han llegado a la etapa de ser probados en humanos (en estudios clínicos). Los esfuerzos para mejorar la mamografía convencional incluyen la mamografía digital (ver la pregunta 14), las imágenes por resonancia magnética (IRM) y la tomografía por emisión de positrones (PET).
Además de las tecnologías de imágenes, científicos apoyados por el Instituto Nacional del Cáncer están explorando métodos para detectar marcadores de cáncer de mama en la sangre, la orina o aspiraciones del pezón (líquido del seno) que puede servir como signo precoz de cáncer de mama. La hoja informativa del NCI: Improving Methods for Breast Cancer Detection and Diagnosis proporciona más información acerca de las tecnologías que se están desarrollando para los exámenes selectivos de detección y el diagnóstico de cáncer de mama. Esta hoja informativa está disponible en http://www.cancer.gov/cancertopics/factsheet/Detection/breast-cancer, o puede ser solicitada al CIS en el teléfono 1–800–422–6237 (1–800–4–CANCER).
¿Qué estudios apoya el Instituto Nacional del Cáncer para encontrar formas mejores de prevenir y tratar el cáncer de mama?
El Instituto Nacional del Cáncer apoya muchos estudios que buscan mejorar la prevención y el tratamiento del cáncer de mama.
• Investigación básica: Los investigadores están trabajando en identificar las causas del cáncer de mama, lo cual incluye el papel de las alteraciones en los genes BRCA1 y BRCA2. Ellos están también estudiando cómo actúan estos genes con otros genes y con factores hormonales, dietéticos y ambientales.
• Prevención: Los investigadores están buscando formas de prevenir el cáncer de mama en mujeres que tienen un riesgo mayor. Para algunas de estas mujeres, se ha mostrado que los fármacos tamoxifeno y raloxifeno reducen el riesgo de padecer cáncer de mama. Otros medicamentos están actualmente en estudio. Además, se están llevando a cabo estudios para evaluar en qué forma la modificación de la dieta, la actividad física, la alimentación y los factores ambientales pueden dar como resultado un riesgo menor de padecer cáncer de mama.
• Detección temprana y diagnóstico: Varios estudios están buscando mejores métodos de detectar y diagnosticar el cáncer de mama para que las mujeres puedan recibir tratamiento más pronto.
• Tratamiento: Varios estudios están enfocados en encontrar tratamientos para el cáncer de mama que sean más efectivos y menos tóxicos que los tratamientos actuales.
Mamografía
La mamografía es un tipo específico de imágenes que utiliza un sistema de dosis baja de rayos X para examinar las mamas. Un examen de mamografía, llamado mamograma, se utiliza para asistir en la detección temprana;y el diagnóstico de las enfermedades mamarias en las mujeres.
Un rayos X (radiografía) es un examen médico no invasivo que ayuda a los médicos a diagnosticar y tratar las condiciones médicas. La toma de imágenes con rayos X supone la exposición de una parte del cuerpo a una pequeña dosis de radiación ionizante para producir imágenes del interior del cuerpo. Los rayos X son la forma más antigua y de uso más frecuente para producir imágenes médicas.
Dos recientes avances a la mamografía tradicional incluyen la mamografía digital y la detección asistida por computadora.
La Mamografía digital, también llamada mamografía digital de campo completo (MDCC), es un sistema de mamografía en el que la película de rayos x es reemplazada por detectores en estado sólido que transforman los rayos X en señales eléctricas. Estos detectores son similares a los que tienen las cámaras digitales. Las señales eléctricas se utilizan para producir imágenes de las mamas que pueden verse en una pantalla de computadora o impresas en una película especial similar a los mamogramas convencionales. Desde el punto de vista del paciente, tener una mamografía digital es esencialmente lo mismo que tener mamograma convencional de pantalla-película.Ver "Mamografía digital de campo completo: ¿Una alternativa potencial a la técnica tradicional de pantalla-película?" bajo el encabezado de las Noticias para obtener mayor información sobre el funcionamiento de la mamografía digital de campo completo y sus potenciales ventajas. -->
Los sistemas de detección asistida por computadora (AC) utilizan una imagen mamográfica digitalizada que puede obtenerse ya sea de un mamograma convencional de película o un mamograma adquirido digitalmente. El software de la computadora entonces busca áreas anormales de densidad, masa o calcificación que puedan indicar la presencia de cáncer. El sistema de detección asistida por computadora resalta estas áreas en las imágenes, alertando al radiólogo de la necesidad de análisis adicionales.
Algunos de los usos comunes del procedimientoLos mamogramas son utilizados como una herramienta de exploración para detectar de manera temprana el cáncer de mamas en las mujeres que no tienen síntomas y para detectar y diagnosticar enfermedades mamarias en mujeres que tienen síntomas tales como bultos, dolor o secreción del pezón.
Mamografía de exploración
La mamografía juega un papel central en la detección temprana del cáncer de mamas ya que puede mostrar los cambios en las mamas hasta dos años antes de que el médico o paciente los adviertan. Las pautas actuales del Departamento de Salud y Servicios Humanos de los Estados Unidos (HHS, por sus siglas en inglés), la Sociedad Estadounidense del Cáncer (ACS, por sus siglas en inglés), la Asociación Médica Estadounidense (AMA, por sus siglas en inglés) y el Colegio Estadounidense de Radiología (ACR, por sus siglas en inglés) recomiendan realizarse una mamografía de exploración cada año en las mujeres, comenzando a partir de los 40 años. La investigación ha demostrado que los mamogramas anuales llevan a la detección temprana del cáncer de mamas, etapa en la que tienen mayores posibilidades de curación y se encuentran disponibles terapias de conservación de mamas.
El Instituto Nacional de Cáncer (NCI, por sus siglas en inglés) agrega que las mujeres que han tenido cáncer de mamas y aquellas que se encuentran en alto riesgo debido a antecedentes genéticos de cáncer de mamas deben asesorarse con un médico especialista respecto de si deben comenzar a realizarse estudios antes de los 40 y sobre la frecuencia de las exploraciones.
Ver la página de Cáncer de Mamas para obtener mayor información sobre la terapia del cáncer de mamas.
Mamografía de diagnóstico
La mamografía de diagnóstico se utiliza para evaluar a una paciente con resultados clínicos anormales—tales como nódulos o bultos en las mamas—descubiertos por la mujer o su médico. La mamografía de diagnóstico también puede realizarse luego de una mamografía de exploración anormal con el fin de evaluar el área conflictiva en el examen de exploración.
volver arriba
Forma en que debo prepararme
Antes de programar un mamograma, la Sociedad Estadounidense del Cáncer (ACS, por sus siglas en inglés) y otras organizaciones de la especialidad recomiendan que discuta cualquier nuevo resultado o problema en las mamas con su médico. Además, informe a su médico sobre cualquier cirugía realizada con anterioridad, uso de hormonas, y antecedentes familiares o personales de cáncer de mamas.
No programe su mamograma para la semana anterior a su período si sus mamas normalmente están sensibles durante este tiempo. El mejor momento para realizar un mamograma es una semana después de su período. Siempre informe a su médico o tecnólogo de rayos X si existe la posibilidad de estar embarazada.
La ACS también le recomienda:
No utilice desodorante, talco en polvo o loción debajo de los brazos o en las mamas el día del examen. Esto puede aparecer en el mamograma como manchas de calcio.
Describa cualquier síntoma o problema en las mamas al tecnólogo que realiza el examen.
Si es posible, obtenga mamogramas anteriores y téngalos a disposición del radiólogo al momento de realizar el examen actual.
Pregunte cuándo estarán disponibles sus resultados: no asuma que los resultados son normales si su médico o el establecimiento de mamografía no se pone en contacto con usted.
volver arriba
Forma en que se ve el equipo utilizado para la mamografía
Una unidad de mamografía consiste en una caja rectangular que contiene el tubo que genera los rayos X. La unidad se utiliza exclusivamente para los exámenes de rayos X en la mama, con accesorios especiales que permiten que sólo la mama se quede expuesta a los rayos X. Conectado a la unidad se encuentra un dispositivo que sostiene y comprime la mama y la posiciona para poder obtener imágenes de diferentes ángulos.
volver arriba
De qué manera funciona el procedimiento
Los rayos X son una forma de radiación, como la luz o las ondas de radio. Los rayos X pasan a través de la mayoría de los objetos, incluso el cuerpo. Una vez que se encuentra cuidadosamente dirigida a la parte del cuerpo a examinar, una máquina de rayos X genera una pequeña cantidad de radiación que atraviesa el cuerpo, produciendo una imagen en película fotográfica, o en una placa especial de registro de imágenes digitales.
Los rayos X son absorbidos por diferentes partes del cuerpo en variables grados. Los huesos absorben gran parte de la radiación mientras que los tejidos blandos, como los músculos, la grasa y los órganos, permiten que más de los rayos X pasen a través de ellos. En consecuencia, los huesos aparecen blancos en los rayos X, mientras que los tejidos blandos se muestran en matices de gris y el aire aparece en negro.
Hasta muy recientemente, las imágenes de rayos X se han mantenido como copia impresa en película (muy similar a un negativo fotográfico). Hoy en día, la mayoría de las imágenes son archivos digitales que se almacenan electrónicamente. Estas imágenes almacenadas son de fácil acceso y a veces se comparan con las imágenes actuales de rayos X para el diagnóstico y la administración de enfermedades.
volver arriba
Cómo se realiza
La mamografía se realiza en pacientes ambulatorios.
Durante la mamografía, un tecnólogo radiológico especialmente calificado posicionará su mama en la unidad de mamografía. La mama será colocada en una plataforma especial y comprimida con una paleta (por lo general hecha de Plexiglas transparente u otro plástico). El tecnólogo comprimirá la mama gradualmente.
La compresión de la mama es necesaria para:
Aplanar el grosor de la mama de manera que todos los tejidos puedan visualizarse.
Extender el tejido de manera que las anormalidades pequeñas son menos probables de quedar oscurecidas por el tejido superior de la mama.
Permitir el uso de una dosis más baja de rayos X ya que una cantidad más delgada de tejido mamario está siendo tomada en imágenes.
Mantener la mama firme con el fin de minimizar lo que se vea borroso en la imagen a causa del movimiento.
Reducir la dispersión de rayos X para aumentar la agudeza de la imagen.
El tecnólogo permanecerá detrás de un escudo de vidrio durante la exposición a los rayos X. Se le solicitará que cambie de posición durante el procedimiento de toma de imágenes. Las visualizaciones de rutina son de arriba hacia abajo y lateral oblicua. El proceso se repetirá para la otra mama.
Usted debe permanecer inmóvil y se le puede solicitar que contenga la respiración por unos segundos mientras se toma la imagen de rayos X para reducir la posibilidad de que ésta resulte borrosa. El tecnólogo se dirigirá detrás de una pared o hacia la sala contigua para activar la máquina de rayos X.
Al completar el examen, se le solicitará a usted que espere hasta que el tecnólogo determine que se hayan obtenido todas las imágenes necesarias.
El proceso de examen tomará aproximadamente 30 minutos.
volver arriba
Qué experimentaré durante y después del procedimiento
Sentirá presión en la mama mientras la paleta de compresión la aprieta. Algunas mujeres con mamas sensibles pueden experimentar incomodidad. Si este es el caso, programe la realización del procedimiento cuando las mamas se encuentren menos sensibles. Asegúrese de informar al tecnólogo si tiene dolor a medida que aumenta la compresión. Si sufre de gran incomodidad, se utilizará menos compresión.
volver arriba
Quién interpreta los resultados y cómo los obtengo
Un radiólogo, un médico específicamente capacitado para supervisar e interpretar los exámenes de radiología, analizará las imágenes y enviará un informe firmado a su médico remitente o de atención primaria, quien compartirá con usted los resultados.
El establecimiento donde se realice la mamografía también le informará de los resultados.
volver arriba
Cuáles son los beneficios y los riesgos
Beneficios
Las imágenes de las mamas mejoran la capacidad del médico de detectar los tumores pequeños. Cuando los tumores son pequeños, la mujer tiene mayores opciones de tratamiento y es mayor la posibilidad de cura.
El uso de la mamografía de exploración aumenta la posibilidad de detección de pequeños crecimientos de tejidos anormales restringidos a los conductos lácteos en las mamas, llamados carcinoma ductal in situ (CDIS). Estos tumores en etapa temprana no pueden dañar a las pacientes si se eliminan en esta fase y la mamografía es el único medio comprobado de detectar de manera confiable estos tumores. También es útil para detectar todos los tipos de cáncer de mamas, incluso el cáncer ductal invasivo y el lobular invasivo.
No queda radiación en el cuerpo de un paciente luego de realizar el examen de rayos X.
Los rayos X por lo general no tienen efectos secundarios en el rango diagnóstico.
Riesgos
Siempre existe una leve probabilidad de tener cáncer como consecuencia de la exposición a la radiación. Sin embargo, el beneficio de un diagnóstico exacto es ampliamente mayor que el riesgo.
La dosis de radiación efectiva de un mamograma es alrededor de 0,7 mSv, que es aproximadamente la misma que una persona promedio recibe de radiación de fondo en tres meses. Las pautas federales sobre la mamografía requieren que todas las unidades sean revisadas por un físico médico cada año para garantizar el correcto funcionamiento de las mismas. Ver la página de Seguridad para obtener mayor información sobre la dosis de radiación.
Mamogramas con resultado falso positivo. Del 5 al 15 por ciento de los mamogramas de exploración requieren de mayor evaluación, como por ejemplo la realización de mamogramas adicionales o ultrasonido. La mayoría de estos exámenes resultan ser normales. Si aparece un resultado anormal, se deberá realizar un seguimiento o biopsia. La mayoría de las biopsias confirman la ausencia de cáncer. Se estima que una mujer que se realizó mamogramas anuales entre los 40 y 49 años cuenta con una probabilidad del 30% de tener un mamograma con resultado falso positivo en algún punto durante esa década y aproximadamente una probabilidad del 7 al 8 % de realizar una biopsia de mamas dentro del período de 10 años.
Las mujeres siempre deberán informar a su médico o al tecnólogo de rayos X si existe la posibilidad de embarazo. Ver la página de Seguridad para obtener mayor información sobre el embarazo y los rayos X.
Sobre la minimización de la exposición a la radiación
Se debe tener especial cuidado durante los exámenes de rayos X en utilizar la mínima dosis posible de radiación y a la vez generar las mejores imágenes para la evaluación. Los concejos nacionales e internacionales de protección de la radiología revisan y actualizan constantemente las normas técnicas utilizadas por los profesionales en radiología.
Los sistemas de vanguardia de rayos X tienen haces de rayos X controlados firmemente y métodos de control de filtración y de dosificación para minimizar la desviación o dispersión de radiación. Esto garantiza que aquellas partes del cuerpo de las que no se toman imágenes reciban la mínima exposición posible a la radiación.
volver arriba
Cuáles son las limitaciones de la mamografía
Las imágenes iniciales mamográficas no siempre son suficientes para determinar con certeza la existencia de una enfermedad benigna o maligna. Si un resultado o una mancha resultan sospechosos, su radiólogo puede recomendarle estudios de diagnóstico adicionales.
Las interpretaciones de los mamogramas pueden resultar difíciles ya que una mama normal puede aparecer diferente para cada mujer. También, el aspecto de una imagen puede verse comprometida si existe polvo o ungüento en las mamas o si se ha realizado una cirugía mamaria. Teniendo en cuenta que es difícil visualizar ciertos cánceres de mamas, el radiólogo puede querer comparar la imagen con imágenes de exámenes previos. No todos los cánceres de mamas pueden visualizarse en una mamografía.
Los implantes mamarios también pueden impedir una lectura exacta del mamograma ya que los implantes salinos y de silicona no son transparentes en los rayos x y puede bloquear la visualización clara de los tejidos detrás de ellos, especialmente si el implante ha sido colocado en frente, en lugar de colocarlo abajo, de los músculos del tórax. Los tecnólogos y los radiólogos con experiencia saben cómo comprimir cuidadosamente las mamas para mejorar la visualización sin romper el implante.
Al acordar una cita para la realización de un mamograma, las mujeres con implantes deben preguntar si el establecimiento utiliza técnicas especiales diseñadas para acomodarlos. Antes de tomar el mamograma, deben asegurarse de que el tecnólogo cuenta con experiencia en la realización de mamografías en pacientes con implantes mamarios.
Mientras que la mamografía es la mejor herramienta de exploración del cáncer de mamas actualmente disponible, los mamogramas no detectan todos los tipos de cáncer de mamas. Asimismo, una pequeña parte de los mamogramas indica que un cáncer posiblemente esté presente cuando no lo es (esto se denomina resultado falso positivo).
La investigación se está realizando en base a una variedad de técnicas de imágenes mamarias que pueden contribuir a la detección temprana del cáncer de mamas y mejorar la exactitud para distinguir entre las condiciones mamarias no cancerosas y los cánceres de mamas.
Tomografia computarizada 3D en displasia acetabular de la cadera en niños y adultos. Nuevas formas de enfocar un diagnostico
El índice de descubrimiento lateral de la cabeza con respecto del acetábulo es la relación de la parte de la cabeza cubierta con respecto al ancho de la cabeza del fémur en una vista radiográfica antero-posterior. En 3DTC se analiza El Porcentaje de Extrusión Lateral de la Cabeza como una medida de la relación que existe entre dos vectores: El primero: comprendido de una línea vertical y perpendicular a la línea bi-isquiática el cual pasa por el borde superior y más externo del acetábulo y el segundo: desde el centro de rotación de la cabeza femoral perpendicular a la línea media; Calculado: (A – B) x 100 / A. Los valores <>
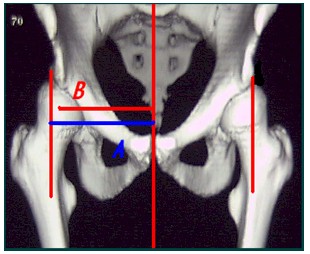
Gráfica nº 7. Porcentaje de extrusión lateral de la cabeza. Medida de la relación que existe entre dos vectores: El primero: comprendido de una línea vertical y perpendicular a la línea bi-isquiática el cual pasa por el borde superior y más externo del acetábulo; y el segundo: desde el centro de rotación de la cabeza femoral perpendicular a la línea media; Calculado: (A – B) x 100 / A, (*N: <>
Figure nº 7. Lateral extrusion percentage (LEP) Measure of the relation that exists between two vectors: the first: comprehend from a vertical and perpendicular line to the bi-isquiatic line which passes by the superior and most external edge of the acetabulum; the second: from the rotation center of the femoral head perpendicular to the medium line; calculated: (a – b) x 100 / a, (*n: <>
El ángulo de cubierta del acetábulo ACM (Índice de Sharp) según Idelberger y Frank, (33) es prácticamente independiente de la torsión e inclinación de la pelvis, formado por la línea que une el borde superior del acetábulo con el borde inferior del mismo formando un ángulo con la línea bi-isquiática. El valor normal en mayores de 19 años es de cuarenta y dos (42°) grados, rango 40°-45° (33, 37) si es mayor nos indicará displasia (Gráfica 8).
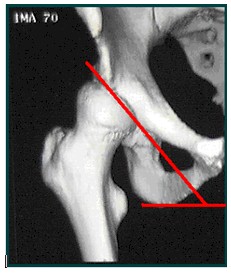
Gráfica nº 8. Índice de Sharp. Se mide con una línea que une el borde superior del acetábulo con el borde inferior del mismo formando un ángulo con la línea bi-isquiática, (*N: 42º).
Figure nº 8. Sharp index. (SI) It’s measured with a line that unites the superior edge of the acetabulum with the inferior edge of the same forming an angle with the bi-isquiatic line, (*n: 42º).
Porcentaje del Acetábulo Medial Desocupado: evaluado en la proyección A- P verdadera centrada en pubis con rotación interna de 15 grados de los miembros inferiores en el 3DTC. Se trazan dos vectores: El primero(A) desde el trasfondo acetabular hasta S2 en la línea media. El segundo (B) desde el centro de la cabeza femoral hasta S2 de la línea media. Calculándose ((B –A) x 100)/B. Valores normales <10%>
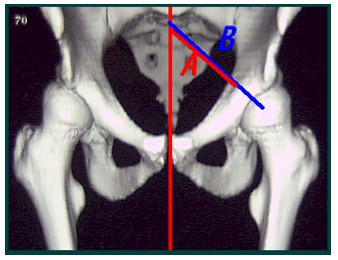
Gráfica nº 9. Porcentaje del acetábulo medial desocupado. Se trazan dos vectores: El primero(A) desde el trasfondo acetabular hasta S2 en la línea media. El segundo (B) desde el centro de la cabeza femoral hasta S2 de la línea media. Calculándose ((B –A) x 100)/B, (*N:<>
Figure nº 9. Percentage of the empty medial acetabulum (PEMA). Two vector are drawn: the first (a) from the acetabular background until s2 in the medium line. The second (b) from the center of the femoral head until s2 of the medial line. Without evidence of medial protrusio acetabuli. Calculated: ((b –a) x 100)/b, (*n:<>
Asimetría del centro de rotación: Medida en la proyección A-P verdadera centrada en pubis con rotación interna de 15 grados de los miembros inferiores del 3DTC, calculándose por una relación que existe al trazar una perpendicular desde los centros de rotación a la línea media, cuya distancia se mide en milímetros. (A – B) x 100 / B + A (Gráfica 10).
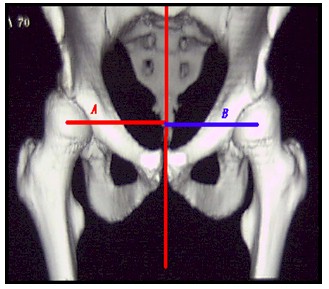
Gráfica nº 10. Simetría del centro de rotación. Es una relación que existe al trazar una perpendicular desde los centros de rotación a la línea media, cuya distancia se mide en milímetros. (A – B) x 100 / B + A. (*N: 0%).
Figure nº 10. Symmetry of the rotation center (SRC). Is a relation that exists when drawing a perpendicular from the centers of rotation to the medium line, its distance is measured in millimeters. (a – b) x 100 / b + a. (*n: 0%).
ANGIOGRAFIA POR TOMOGRAFIA AXIAL COMPUTADA ( Angio TAC)
Ventajas:
1.- | Es un estudio rápido, sencillo y no invasivo. |
2.- | Adquiere volúmenes completos del cuerpo. Por ello, obtiene imágenes multiplanares y tridimensionales, clarificando lesiones complejas propias o adyacentes a las arterias que se estudian. |
3.- | Se acerca bastante a la precisión de la angiografía por sustracción digital. |
Desventajas:
1.- | Utiliza radiaciones ionizantes (rayos X) |
2.- | Usa volúmenes de contraste iodado que pueden producir reacciones alérgicas o nefrotoxicidad. |
3.- | El grado de enfermedad y calcificación de las paredes arteriales limitan la evaluación debido a condicionar alteraciones del flujo arterial o artefactos radiantes ( brillantes) respectivamente. |
4.- | El tiempo de adquisición de la imagen debe ser preciso para la exactitud de la evaluación, si no la información es variable debido al retorno venoso. |
5.- | Al igual que en la Angio RMN, a menor diámetro y flujo arterial, menor posibilidad de obtener una imagen anatómica adecuada y diagnostica. |
Figura # 1. Angio TAC con reconstruccion 3D –“ volume rendering”en proyección oblicua y en blanco –negro para evaluar angiografía aortica. Hay evidencia de tortuosidad arterial moderada y aneurisma pequeño infrarenal. Se pueden apreciar la relación con los huesos de la columna vertebral. |  |
 | Figura # 2. Paciente masculino de 65 años con arteriosclerosis severa tortuosidad, dilatación y múltiples placas de ateromas calcificadas. Se observa aneurisma (flecha) entre las arterias renales y bifurcación iliaca. Figura # 2-A. Angio TAC en adquisición de superficie sombreada ( SSD) permite apreciar mejor la distribución de las calcificaciones. |
Figura # 2-B. Angio TAC del mismo paciente en imagen 3-D “volume rendering” a color, evaluando la vista posterior de la dilatación aneurismática pero eliminando la columna vertebral y dejando sólo la opacificación aòrtica, por medio del trabajo computadorizado de unos 30 minutos de duración. |  |
 | Figura # 3. Demuestra Angio TAC de aorta en otro paciente con aneurisma de aorta abdominal por debajo de las arterias renales. La adquisición es volumétrica y en imagen 3-D “volume rendering” en blanco y negro, habiendo eliminado computerizadamente los huesos. Nótese los detalles angiograficos de las arterias renales y mesentéricas ( flechas) |
Figura # 4. Paciente masculino de 70 años con antecedentes diabetes y fumador con clínica de EAPO. Angio TAC en imágenes multiplanares demuestra enfermedad arteriosclerótica severa tipo III con múltiples placas, tortuosidad, dilatación e irregularidad importante de las paredes arteriales. Figura # 4-A. Angio TAC en segmento largo aorto-iliaco femoral desde las arterias renales hasta tercio medio de los muslos. Hay estenosis pre-oclusiva en el origen de la arteria iliaca derecha ( flechas) y enfermedad moderada en arterias femorales. |  |
 | Figura # 4-B. Angio TAC desde el tercio medio de los muslos hasta los pies demuestra enfermedad moderada en arterias femorales y poplíteas. Hay enfermedad severa distal con oclusión completa de ambas arterias tibiales anteriores(flechas largas) y posteriores (flechas cortas) Las arterias peroneas presentan se opacifican hasta el nivel de los tobillos. |
Vasculares
Durante el siguiente caso clínico, se utilizaron el sistema de Angiografía con sustracción digital y la tecnología de reconstrucción 3D/CT de Innova durante el tratamiento de un aneurisma hipogástrico izquierdo roto con un stent.
Historial del paciente
Este es el caso de un varón de 63 años de edad con un historial de fibrilación auricular que está tomando una medicación de Warfarin.El modo de adquisición de Innova CT es útil para evaluar los hematomas retroperitoneales lo cual evita el traslado del paciente a un escáner tomográfico normal. Utilizaremos esta aplicación, especialmente en aquellos casos que implique la rotura de las arterias ilíacas durante la angioplastia trasluminal percutánea (PTA)/stent para las enfermedades de aterosclerosis obliterativa.
Procedimiento
Meningiomas del ala esfenoidal
Clasificación.-
según Bonnal:
Grupo A:
clinoidales Se extienden desde la duramadre del seno cavernoso, clinoides anteriores y parte interna del ala del
esfenoides. En contacto con nervios ópticos, arteria carótida y sus ramas
Grupo B:
en placa del ala Producen hiperostosis ósea y la placa crece en la del esfenoides duramadre del ala y seno cavernoso. La arteria carótida y sus ramas no están afectadas. El nervio óptico puede estar comprimido
Grupo C:
en masa del ala Combina los grupos A y B. Son muy invasivos del esfenoides y crecen hacia la línea media y el clivus
Grupo D:
del borde medio No invasivos. Inserción dural pequeña. Sin conexión del esfenoides con la arteria carótida ni con los nervios ópticos
Grupo E:
Pterional: Parte externa del ala del esfenoides en el límite entre la base y la convexidad. Se hallan en la cisura
silviana distorsionando los lóbulos frontal y temporal.
Nakamura divide los de 1/3 medio en 2 grupos
Grupo 1 sin afectación de seno cavernoso
Grupo 2 con afectación de seno cavernoso, siendo estos más frecuentes.
Epidemiología.-
Ésta es la localización más frecuente entre los meningiomas de la base del cráneo y constituyen aproximadamente el 18% de todos los meningiomas intracraneales. Clásicamente se han distinguido tres variedades, según se afecte la región más interna o externa del ala del esfenoides: tercio interno, tercio medio y tercio externo.
Son más frecuentes en pacientes del sexo femenino en la década de los 50 años de edad.
Clínica.-
La duración media de los síntomas es de aproximadamente 3 años.
La escala clínica más recomendable es la de Karnofsky y se precisa un estudio oftalmológico preoperatorio.
Los síntomas más comunes pueden variar entre epilepsia, alteraciones del carácter y cefaleas, también .disminución de la agudeza visual, edema de papila y atrofia de papila. Afectación del V par , III par , pérdida de memoria, bradipsiquia,depresión y disfasia motora.
Anatomía Patológica.-
La mayoría son meningoteliales o psammomatosos.Pueden presentar distintos grados de calcificación o hialinosis.
Diagnóstico.-
La RM es la técnica primaria para diagnosticar meningiomas:
Delinea el nivel del tumor y la relación del tumor con el parénquima cerebral. Las imágenes son hipo o isointensas en T1 e hiperintensas en T2, con captación de contraste irregular, debido a la presencia de cuerpos de psamoma.
En algún caso la imagen de hipointensidad es más evidente por la gran cantidad de calcio intratumoral.
Se visualiza la característica imagen de pseudocápsula de LCR en casi todos los casos.
Asimismo se observa imagen de cola dural en casi todos ellos y a veces de forma muy evidente.
Pueden presentar edema importante y se corresponde con tumores de diámetro mayor.

Se precisa TAC de cráneo. En algunos casos se observan hiperostosis de la base y calcificaciones intratumorales.
En las imágenes de la angiografía cerebral dependiendo del tamaño se pueden apreciar desplazamientos y atrapamientos vasculares.Las arterias nutricias proceden de la carótida interna, carótida externa, ramas de la meníngea media y ramas de la maxilar interna.
Tratamiento.-
Técnica quirúrgica
Craneotomías pterionales o según expansión craneotomías frontotemporales con fresado del techo de la órbita, ala menor del esfenoides y clinoides anteriores, según técnica de Dolenc y AlMefty, acompañado de la resección extradural de hueso infiltrado (Schick, Bleyen et al. 2006).
Exéresis tumoral.
Se consiguen generalmente resecciones de grado 1 y 2 de Simpson, aunque algunas veces la extirpación solo es subtotal.
Pronóstico.-
Como complicaciones más frecuentes se pueden producir paresias del III - V par y hemiparesias que suelen ser transitorias. Crisis epilépticas postoperatorias y fístula de LCR , trombosis venosa profunda y tromboflebitis, diabetes transitoria y neumonía.
El pronóstico es más favorable en aquellos sin afectación del seno cavernoso.Los trastornos de visión mejoran en un 50 % de los casos (Nakamura, Roser et al. 2006).
Su recurrencia puede llegar a ser del 30% (Korshunov,Cherekaev et al. 2007) y está en relación a la invasión ósea (Roser, Nakamura et al. 2005).
ENFERMEDAD CEREBROVASCULAR
La enfermedad cerebrovascular o vascular cerebral, como también se le conoce, (EVC o AVC) se refiere a todas aquellas entidades que lesionan a las estructuras intracraneales debido a alteraciones de los vasos sanguíneos ya sea en forma directa o indirecta.
Es decir, para que hablemos de EVC es indispensable que la lesión del encéfalo este dada como consecuencia de una afección a sus vasos sanguíneos, como por ejemplo la ruptura de los mismos como en el caso de las hemorragias ("derrames"), o la oclusión de las arterias que provoca infartos, etc.
Con fines didácticos, es necesario dividir a los EVC’s en oclusivos y hemorrágicos, ya que de inicio es de suma importancia saber si el evento que se presenta es de una u otra de estas dos clases. La importancia radica en que la identificación precisa del evento dicta el tratamiento inicial mismo que, si es adecuado determinará si un paciente sobrevive en primera instancia, y ulteriormente si es así, si el paciente quedará o no con secuelas.
La piedra angular en la identificación de un caso con EVC es la historia clínica en primera instancia seguida de la exploración del paciente, una vez que se ha demostrado que el paciente tiene una afección aguda del sistema nervioso entonces se deberá proceder siempre a la realización de una tomografía axial computada (TAC) de cráneo, la cual determinará con una especificidad del 100% si se trata de un evento oclusivo o hemorrágico.
Una vez demostrado lo anterior se procederá a la terapia de urgencia y al mismo tiempo, cuando las condiciones del enfermo lo permitan, a la realización de estudios auxiliares para intentar demostrar la causa subyacente del evento. No todos los EVC’s ocurren a pacientes añosos, no todos los EVC’s son por alteraciones propias de los vasos intracraneales "por la edad", es por esto que hay que conocer las diferencias en distribución temporal de las diferentes afecciones vasculares al encéfalo.
Dentro del apartado de las hemorragias, tenemos las más frecuentes que son las de los hipertensos, estas ocurren con mayor frecuencia en las 6º y 7º décadas de la vida, habitualmente asociadas a actividad física o esfuerzo y la presentación típica es con cefalea súbita y/o pérdida de la conciencia en forma aguda y datos de focalización. Esto no quiere decir que en otro tipo de eventos no existan estos datos, pero sí son mas frecuentes en las hemorragias.
Otro tipo de hemorragia es la que ocurre en personas de entre 30 y 50 años, en los que hay cefalea súbita asociada a esfuerzo y que encontramos signos meníngeos francos, estamos ante una hemorragia subaracnoidea (HSA). Es de suma importancia determinar la existencia de HSA puesto que la atención neuroquirúrgica de emergencia es imperativa.
En el caso de los eventos oclusivos, estamos acostumbrados a pensar en las trombosis o embolias como enfermedades de "viejitos" y no siempre es así.
Es tan frecuente que ante un caso de déficit neurológico que se presenta de manera paulatina rápidamente progresiva sin necesariamente pérdida de la conciencia uno no le de la importancia que merece, y la realidad es que se trata de una emergencia médica, cualquier paciente con inicio de déficit neurológico que progresa es imperativo su internamiento, realización de TAC de cráneo y manejo en etapa aguda, ulteriormente se deberán realizar estudios para tratar de encontrar la causa de su evento oclusivo, es por una arritmia, por bajo gasto cardiaco, por placa de ateroma en carótidas, por fenómeno de robo por una malformación vascular cerebral, etc
Es así pues que debemos seguir la siguiente ruta crítica ante un enfermo con cuadro neurológico agudo o de recién inicio:

Es así que la necesidad de TAC de cráneo de urgencia es de suma importancia, puede imaginar lo que sucedería si a un enfermo con evento hemorrágico, le iniciamos medidas antitrombóticas empíricamente, es decir sin TAC.
Hay que recordar siempre, que la única justificación para no hacer TAC de cráneo de urgencia es que el único gabinete de tomografía quede a 500Km de distancia de donde se encuentra el enfermo, y entonces deberá de procederse al traslado pronto para la atención del enfermo.










